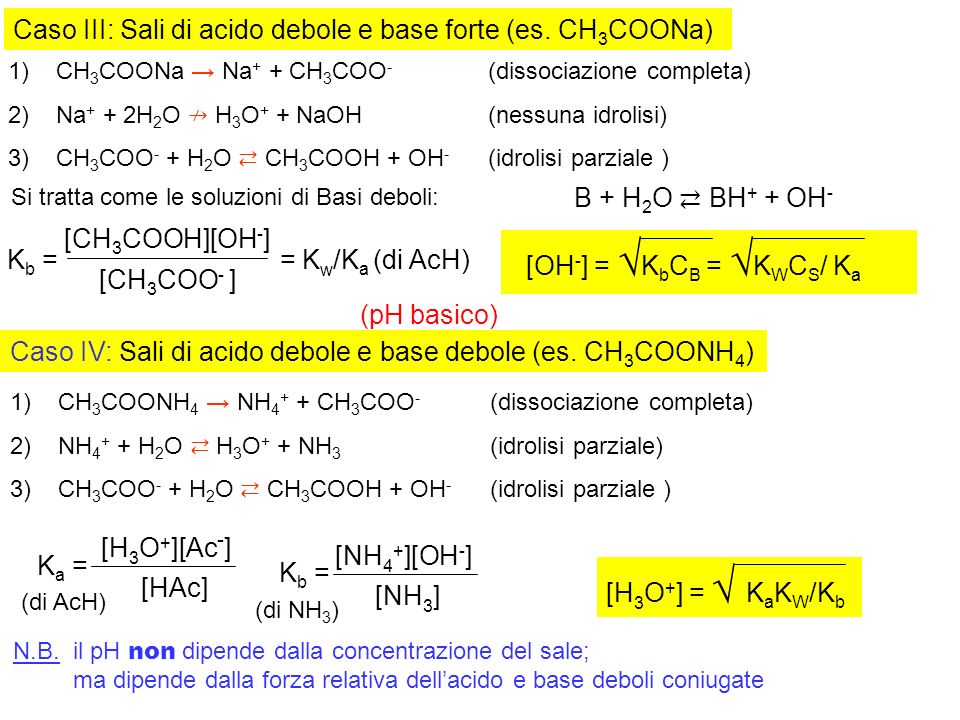
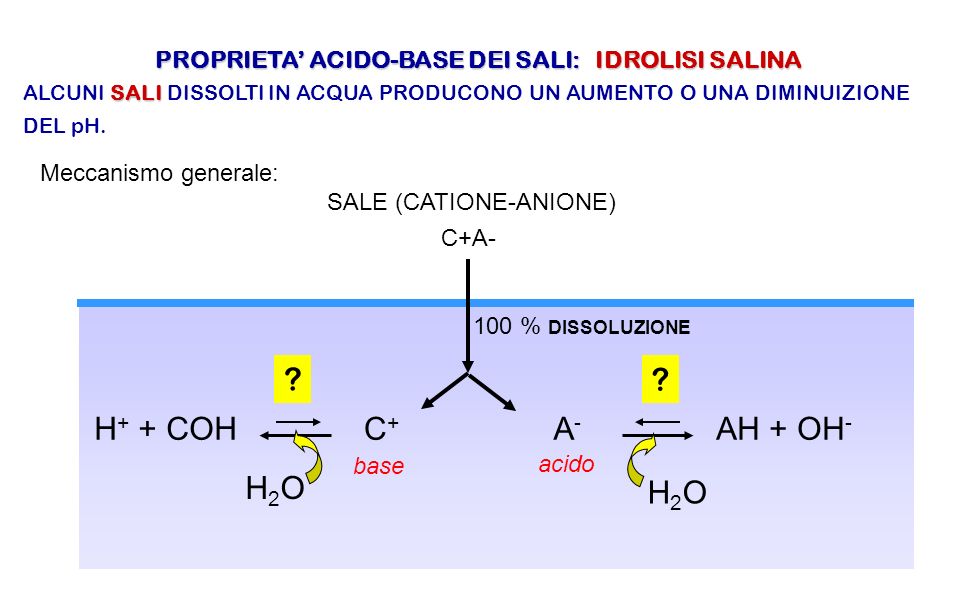
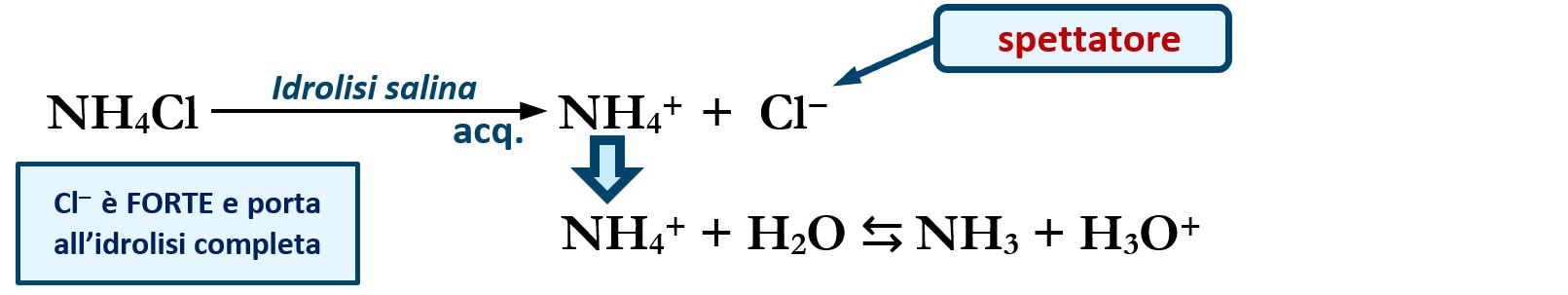Il pH della soluzione di un sale Caso I: Sali di acido forte e base forte (es. NaCl) 1)NaCl → Na + + Cl - (dissociazione completa) 2)Na + + 2H 2 O ↛ H. - ppt scaricare

1401 19 idrolisi tamponi - Sali come acidi o basi: Idrolisi NaOH + HCl → NaCl + H 2 O 3 Ca(OH) 2 + 2 - Studocu